刷个短视频,随手测个体质,结果被大数据精准 “确诊”:心气受损、心脉不畅。一时间,胸闷心慌、提不起劲、压力大到喘不过气的感受瞬间被戳中,不少人直呼 “世另我”。有人觉得这是网红养生的噱头,可为什么越来越多人会有这种身体感受?抛开玄学的解读,从现代医学的角度深究,这所谓的 “心气心脉受损”,根本不是矫情,而是身体被长期压力、不良作息透支后,发出的真实健康预警,而这一切的核心诱因,藏在我们每个人的日常里。
不知从什么时候开始,我们的身体总处于一种 “紧绷状态”:上班时被工作 KPI 追着跑,下班刷短视频停不下来,睡前还在纠结未完成的琐事,熬夜、焦虑、久坐不动成了常态。这些看似不起眼的日常,却在悄悄触发身体的 “应激开关”,让压力激素皮质醇持续飙升,一边直接影响心血管系统,让心肌收缩功能受干扰,引发胸闷、心悸、胸口发闷的 “心脉受损” 感;一边抑制免疫细胞活性,打乱炎症平衡,让身体出现乏力、易疲劳、精神萎靡的 “心气不足” 表现。
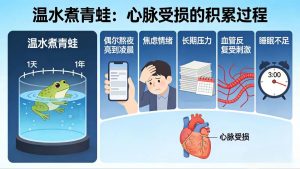
更关键的是,这种损伤并非一蹴而就,而是 “温水煮青蛙” 式的累积。你以为的偶尔熬夜、一次焦虑,身体都在默默记账:长期压力会让血管内皮反复受炎症因子刺激,加速血管老化;睡眠不足会让心脏和免疫细胞失去修复时间;久坐不动则会让血液循环变慢,加重身体的 “淤堵” 感。这就是为什么中医说的 “心气心脉受损”,总能精准戳中现代人的健康痛点 —— 它不是抽象的体质概念,而是压力、作息、生活方式共同作用下,心血管和免疫功能双重失衡的直观体现。
很多人被 “确诊” 后,第一反应是跟风喝养生茶、泡枸杞水,可盲目进补往往治标不治本。因为你连自己的 “心气心脉受损” 到底到了什么程度,核心问题出在哪都不清楚:是天生对压力更敏感?还是免疫失衡引发了慢性炎症?亦或是心血管指标已经出现了隐形异常?仅凭体感判断,只能缓解一时的焦虑,却无法从根源解决问题。

想要真正摆脱这种 “身心俱疲” 的状态,关键不是跟风养生,而是先精准摸清身体的 “压力家底”,再做针对性的调理。这也是为什么越来越多人开始重视科学的压力与免疫评估,而潘道生物的抗压力专项检测,正是为破解这一问题而来,从根源上帮你找到 “心气心脉受损” 的核心症结。
潘道生物的抗压力检测,跳出了传统的情绪评估和体感判断,通过基因检测、免疫功能分析、分子指标检测三大核心模块,实现对身体压力耐受能力、心血管健康状态、免疫平衡水平的精准解码:从基因层面,解析与压力应对、情绪调节相关的基因位点,明确你对压力的先天敏感度,知道自己为何比别人更容易焦虑、心慌;从免疫层面,通过流式细胞术精准检测 T/B/NK 细胞亚群比例,量化炎症因子水平,判断免疫失衡是否在持续损伤心血管;从分子层面,检测皮质醇、心肌酶等关键指标,直观看到压力对心脉、脏腑的实际影响,让 “心气心脉受损” 从模糊的体感,变成可量化、可解读的科学数据。

基于这份精准的检测报告,潘道生物还会为你定制个性化的全周期干预方案:针对长期熬夜、压力大的职场人,制定 “30 分钟中等强度运动 + 睡前 1 小时远离电子设备” 的减压作息,搭配优质蛋白、抗炎营养素的饮食建议,从生活方式入手降低皮质醇水平,缓解心脉负担;针对过敏体质、有免疫家族史的人群,通过营养调理优化免疫细胞活性,减少炎症对血管的持续刺激,改善心气不足的状态;针对高血压、糖尿病等慢病患者,实时监测免疫与心血管指标,避免压力叠加慢病加重心脉损伤。
同时,潘道生物的健康守护不止于检测和干预,更构建了 “检测 – 解读 – 干预 – 监测” 的全周期闭环服务 ,定期跟踪你的压力耐受能力、免疫功能和心血管健康变化,动态调整调理方案,让 “养心脉、补心气” 不再是一句养生口号,而是可执行、可落地的科学健康管理。无论是被短视频 “确诊” 心气心脉受损的年轻职场人,还是反复乏力、易感染的亚健康人群,亦或是关注健康、想提前规避心血管风险的中老年朋友,都能通过这套体系,从根源上摆脱压力带来的身体损伤,让胸闷、心慌、易疲劳的感受彻底远离。
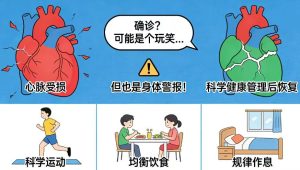
刷短视频被 “确诊” 或许是个玩笑,但身体发出的预警从不会骗人。所谓的心气受损、心脉不畅,不过是身体在提醒你:该停下盲目硬扛的脚步,认真关注自己的压力状态和健康了。与其跟风养生、焦虑内耗,不如用一次科学的检测,摸清身体的真实情况,用精准的调理守护心脉通畅、免疫强健。潘道生物的抗压力专项检测,帮你读懂身体的压力信号,从根源上告别 “心气不足、心脉不畅”,让每一个人都能在快节奏的生活里,拥有健康的身心状态。

