以下是每个阶段的详细分解:
第一阶段:咨询与知情同意 (Pre-Test Counseling & Consent)
这是最关键的第一步,决定了整个检测的方向和伦理基础。
-
专业咨询 (Genetic Counseling):
-
目的: 通常由医生或遗传咨询师进行,目的是评估检测的必要性和合理性。
-
内容: 医生会详细了解个人和家族的疾病史(如癌症、遗传病、心血管疾病等),评估遗传风险,并解释基因检测可能带来的好处、局限性和风险(如心理压力、家庭关系影响、保险和就业歧视等)。
-
-
选择检测项目:
-
根据咨询情况,选择最合适的检测项目。种类繁多,例如:
-
诊断性检测: 用于确认疑似遗传病的诊断。
-
携带者筛查: 检查是否携带某种遗传病的隐性基因,适用于备孕或孕期夫妇。
-
产前筛查/诊断: 如NIPT(无创DNA产前检测)或羊水穿刺,用于筛查胎儿染色体异常。
-
肿瘤基因检测: 针对癌症患者,寻找靶向药物治疗靶点或评估遗传性癌症风险(如BRCA基因)。
-
药物基因组学检测: 了解个体对特定药物的代谢和反应,指导精准用药。
-
健康风险筛查与特质检测: (如23andMe、Ancestry.com提供的消费级检测) 评估某些疾病的风险或了解祖源信息。
-
-
-
签署知情同意书 (Informed Consent):
-
在充分了解所有信息后,受检者需要签署一份知情同意书。这表明受检者自愿进行检测,并理解检测的目的、潜在结果、风险、费用以及隐私保护措施等。这是法律和伦理上的强制要求。
-
第二阶段:样本采集与运送 (Sample Collection & Transportation)
-
采集方法: 根据检测类型,采集不同的生物样本。最常见的是:
-
唾液样本 (Saliva): 消费级基因检测和最常用的无创采集方式。受检者向专用采集管中吐入口水即可,内含稳定液以保护DNA。
-
血液样本 (Blood): 医疗级检测的金标准。由专业医护人员通过静脉穿刺采集,放入抗凝管中。
-
口腔拭子 (Buccal Swab): 用棉签在口腔内壁轻轻刮取脱落细胞。
-
组织样本 (Tissue): 对于肿瘤检测,可能需要手术切除的肿瘤组织(石蜡切片)或进行活检。
-
其他样本: 羊水、绒毛膜、毛发等(特定情况下使用)。
-
-
样本标记与运送:
-
样本容器上会有唯一的条码标识,确保与受检者信息准确对应,同时保护隐私。
-
样本通常会放入稳定的包装中,并通过冷链(低温)运输尽快送到实验室,以保证生物材料的质量。
-
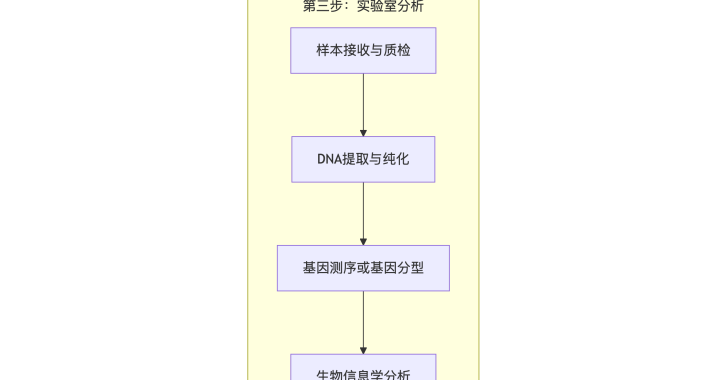
第三阶段:实验室分析 (Laboratory Analysis)
这是技术在实验室里发挥作用的核心环节。
-
样本接收与登记:
-
实验室收到样本后,核对信息,检查样本质量(如唾液量是否足够、血液是否溶血),合格后方会进入下一流程。
-
-
DNA提取与纯化 (DNA Extraction):
-
从细胞中分离出DNA,并去除蛋白质、RNA等杂质,得到高纯度的DNA样本。
-
-
DNA量化与质控 (Quantification & QC):
-
测量提取出的DNA浓度和质量,确保其符合后续检测的要求。
-
-
基因分析 (Genetic Analysis):
-
这是最关键的技术步骤,方法取决于检测目的:
-
基因分型 (Genotyping): 检测特定位置的基因变异(SNPs)。适用于消费级检测和某些疾病风险筛查。速度快,成本低。
-
基因测序 (Gene Sequencing):
-
Sanger测序 (第一代测序): 精准检测一个或几个特定基因的序列,是金标准,但通量低。
-
下一代测序 (Next-Generation Sequencing, NGS): 也称为高通量测序。可以同时对数百万个DNA片段进行测序,是目前主流的临床检测技术。
-
Panel测序: 同时检测一组相关的基因(如几十个与癌症相关的基因)。
-
全外显子组测序 (Whole Exome Sequencing, WES): 检测所有编码蛋白质的基因(约占基因组的1%)。
-
全基因组测序 (Whole Genome Sequencing, WGS): 检测几乎100%的基因组序列,包含编码和非编码区,信息最全,成本最高。
-
-
-
-
-
生物信息学分析 (Bioinformatics Analysis):
-
测序仪器产生的是海量的原始数据(ATCG碱基序列)。生物信息学家通过专门的软件和数据库进行:
-
序列比对 (Alignment): 将测出的序列片段与人类参考基因组进行比对。
-
变异识别 (Variant Calling): 识别出与参考基因组不同的地方(变异)。
-
注释与筛选 (Annotation & Filtering): 解读这些变异的意义:它位于哪个基因?是否会导致氨基酸改变?是已知的致病突变还是无害的多态?这一步需要比对庞大的临床数据库(如ClinVar, gnomAD等)。
-
-
第四阶段:报告撰写与审核 (Report Generation & Interpretation)
数据必须被转化为临床可用的信息。
-
结果解读 (Interpretation):
-
由经过专业训练的分子遗传学家或病理学家对生物信息学分析出的变异进行最终解读。他们会根据美国医学遗传学与基因组学学会 (ACMG) 等机构制定的指南,将变异分类为:
-
致病 (Pathogenic)
-
可能致病 (Likely Pathogenic)
-
意义不明确 (Variant of Uncertain Significance, VUS)
-
可能良性 (Likely Benign)
-
良性 (Benign)
-
-
VUS 是最常见也最令人困惑的结果,意味着目前证据不足以判断其好坏,通常不建议作为临床决策的依据。
-
-
报告生成 (Report Generation):
-
生成一份正式的、易于理解的检测报告。报告通常包括:
-
受检者基本信息
-
检测项目名称和方法(如NGS Panel)
-
检测结果摘要(阳性/阴性/VUS)
-
详细发现的变异及其解读
-
对结果的临床意义说明
-
建议 (Recommendations): 例如建议进行家族验证、采取某些预防措施、更改治疗方案或进行遗传咨询。
-
-
-
报告审核与签发:
-
报告需由另一位专家审核以确保准确性,最终签字签发。
-
第五阶段:结果告知与遗传咨询 (Post-Test Counseling & Follow-up)
最后一步同样至关重要,确保信息被正确理解和使用。
-
结果告知:
-
由最初的医生或遗传咨询师将报告结果告知受检者。他们会用通俗易懂的语言解释报告的含义,避免误解(特别是对于VUS结果)。
-
-
遗传咨询:
-
讨论结果对个人健康、家族成员健康的影响。
-
提供心理支持,应对可能出现的焦虑、恐惧或内疚等情绪。
-
指导下一步行动,如制定个性化的疾病筛查计划、预防性手术、治疗方案、或建议哪些家庭成员也可以进行验证性检测(家族 cascade screening)。
-
-
随访 (Follow-up):
-
科学在不断进步,今天的VUS未来可能被重新分类。一些实验室或诊所会提供随访服务,通知受检者关于其结果的更新信息。
-